HỌC VIỆN HOÀNG GIA
CÂU HỎI
Trộn 200 ml dung dịch HNO3 0,1M vào 200 ml dung dịch NaOH 0,3M thu được 400 ml dung dịch X có giá trị pH là
ĐỀ THI
Câu hỏi thuộc đề thi: Bộ 30 đề thi học kì 1 Hóa 11 có đáp án
LỜI GIẢI
Chọn đáp án A
Phương pháp giải:
Vì HNO3 và NaOH đều là chất điện li mạnh nên ta có: nH+ = nHNO3 và nOH- = nNaOH
PT ion: OH- + H+ → H2O
Tính theo PT ion.
Giải chi tiết:
Vì HNO3 và NaOH đều là chất điện li mạnh nên ta có: nH+ = nHNO3 = 0,02 mol và nOH- = nNaOH = 0,06 mol
PTHH: OH- + H+ → H2O
Bđ: 0,02 0,06 mol
Pư: 0,02 → 0,02 mol
Sau: 0 0,04 mol
→ [OH-] = 0,04 : 0,4 = 0,01 mol → pOH = - log[OH-] = 2 → pH = 14 - pOH = 12
CÂU HỎI CÙNG BÀI THI
Hoà tan hoàn toàn 2,4 gam kim loại M vào dung dịch HNO3 loãng dư thu được 448 ml khí N2 (đktc, sản phẩm khử duy nhất). Kim loại M là
Cho 44,0 gam NaOH vào dung dịch chứa 39,2 gam H3PO4. Sau khi phản ứng xảy ra hoàn toàn, sản phẩm thu được và khối lượng tương ứng lần lượt là
Cho 29 gam hỗn hợp gồm Al, Cu, Ag tác dụng vừa đủ với V lít dung dịch HNO3 1,5M, thu được dung dịch chứa 174,04 gam muối và 5,6 lít (đktc) hỗn hợp X gồm hai khí không màu không hóa nâu ngoài không khí. Tỉ khối của X so với H2 bằng 18,8. Giá trị của V là
Cho các phản ứng sau:
(1) 2NH3 + H2SO4 → (NH4)2SO4.
(2) 4NH3 + 3O2 → 2N2 + 6H2O.
(3) 2NH3 + 3Cl2 → N2 + 6HCl.
(4) 3NH3 + 3H2O + Al(NO3)3 → Al(OH)3 +3NH4NO3.
(5) 4NH3 + 5O2 → 4NO + 6H2O.
(6) 2NH3 + 3CuO → 3Cu + 3N2 + 3H2O
Các phản ứng trong đó NH3 có tính khử là
Cho các phản ứng sau:
(1) 2NH3 + H2SO4 → (NH4)2SO4.
(2) 4NH3 + 3O2 → 2N2 + 6H2O.
(3) 2NH3 + 3Cl2 → N2 + 6HCl.
(4) 3NH3 + 3H2O + Al(NO3)3 → Al(OH)3 +3NH4NO3.
(5) 4NH3 + 5O2 → 4NO + 6H2O.
(6) 2NH3 + 3CuO → 3Cu + 3N2 + 3H2O
Các phản ứng trong đó NH3 có tính khử là
Dẫn luồng khí CO dư qua ống sứ chứa hỗn hợp Al2O3, CuO, MgO, Fe2O3 đun nóng, sau khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm
Một dung dịch có a mol NH4+, b mol Mg2+, c mol SO42- và d mol HCO3-. Biểu thức nào biểu thị sự liên quan giữa a, b, c, d là
Trong phòng thí nghiệm, để điều chế một lượng nhỏ khí X tinh khiết, người ta đun nóng dung dịch amoni nitrit bão hoà (NH4NO2). Khí X là
Hiện tượng "hiệu ứng nhà kính" làm nhiệt độ Trái Đất nóng lên, làm biến đổi khí hậu, gây hạn hán, lũ lụt, nước biển dâng,… Tác nhân chủ yếu gây "hiệu ứng nhà kính" là do sự tăng nồng độ trong không khí quyển của chất nào sau đây?
Cho phương trình phản ứng: Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O, phương trình ion thu gọn ứng với phản ứng trên là
Tiến hành các thí nghiệm sau:
1. Cho dung dịch NH3 vào dung dịch AlCl3.
2. Cho dung dịch AgNO3 vào dung dịch Na3PO4.
3. Cho dung dịch AgNO3 vào dung dịch H3PO4.
4. Cho dung dịch NaOH cho đến dư vào dung dịch Ca(HCO3)2.
5. Cho dung dịch (NH4)2SO4 vào dung dịch NaOH đun nhẹ.
6. Cho dung dịch (NH4)2SO4 vào dung dịch Ba(OH)2 đun nhẹ.
7. Cho dung dịch Fe2(SO4)3 vào dung dịch Ba(OH)2.
8. Cho dung dịch H2SO4 vào dung dịch Ba(HCO3)2.
Sau khi kết thúc thí nghiệm, số trường hợp thu được kết tủa là
Tiến hành các thí nghiệm sau:
1. Cho dung dịch NH3 vào dung dịch AlCl3.
2. Cho dung dịch AgNO3 vào dung dịch Na3PO4.
3. Cho dung dịch AgNO3 vào dung dịch H3PO4.
4. Cho dung dịch NaOH cho đến dư vào dung dịch Ca(HCO3)2.
5. Cho dung dịch (NH4)2SO4 vào dung dịch NaOH đun nhẹ.
6. Cho dung dịch (NH4)2SO4 vào dung dịch Ba(OH)2 đun nhẹ.
7. Cho dung dịch Fe2(SO4)3 vào dung dịch Ba(OH)2.
8. Cho dung dịch H2SO4 vào dung dịch Ba(HCO3)2.
Sau khi kết thúc thí nghiệm, số trường hợp thu được kết tủa là
Cho các kim loại sau: Mg, Al, Cu, Ag, Fe, Au, Zn, Ca. Số kim loại tác dụng được với dung dịch HNO3 đặc nguội là
Cho phương trình phản ứng: Mg + HNO3 → Mg(NO3)2 + NO + H2O.
Tổng hệ số cân bằng (số nguyên tối giản) của các chất trong phản ứng trên là
Cho phương trình phản ứng: Mg + HNO3 → Mg(NO3)2 + NO + H2O.
Tổng hệ số cân bằng (số nguyên tối giản) của các chất trong phản ứng trên là
Trộn 200 ml dung dịch HNO3 0,1M vào 200 ml dung dịch NaOH 0,3M thu được 400 ml dung dịch X có giá trị pH là
Trên bề mặt của vỏ trứng gia cầm có những lỗ nhỏ nên vi khuẩn có thể xâm nhập được và hơi nước, cacbon đioxit có thể thoát ra làm trứng nhanh hỏng. Để bảo quản trứng lâu hỏng, người ta thường nhúng trứng vào dung dịch Ca(OH)2, phản ứng hóa học xảy ra trong quá trình này là
Cho 23,82 gam hỗn hợp X gồm bột Zn và Mg (tỉ lệ mol theo thứ tự là 5:3) tan vừa đủ trong hỗn hợp dung dịch gồm NaNO3 và NaHSO4 thu được dung dịch Y chỉ chứa m gam hỗn hợp các muối trung hòa và 4,704 lít hỗn hợp khí Z (đktc) gồm hai khí không màu, trong đó có một khí hoá nâu trong không khí. Tỉ khối của Z so với H2 là 13. Giá trị m gần nhất là
Dung dịch X chứa các ion: Fe2+ (0,1 mol), Al3+ (0,2 mol), Cl‑(0,3 mol), SO42- (x mol). Giá trị của x là
Dung dịch X có chứa 0,3 mol Na+; 0,1 mol Mg2+; 0,2 mol Cl‑ và x mol NO3-. Khối lượng muối trong dung dịch X là
Các hình vẽ bên dưới mô tả một số phương pháp thu khí thường tiến hành ở phòng thí nghiệm. Cho biết từng phương pháp (1), (2), (3) có thể áp dụng để thu được khí nào trong các khí sau: O2, Cl2, HCl, NH3, SO2, H2(biết rằng một chất khí có thể thu bằng nhiều phương pháp)?
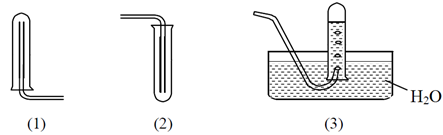
Các hình vẽ bên dưới mô tả một số phương pháp thu khí thường tiến hành ở phòng thí nghiệm. Cho biết từng phương pháp (1), (2), (3) có thể áp dụng để thu được khí nào trong các khí sau: O2, Cl2, HCl, NH3, SO2, H2(biết rằng một chất khí có thể thu bằng nhiều phương pháp)?

Nhiệt phân hoàn toàn m gam Cu(NO3)2 thu được tổng thể tích khí là 5,376 lít (ở điều kiện tiêu chuẩn). Giá trị của m là
Hòa tan hoàn toàn m gam Al vào dung dịch HNO3 loãng, dư thu được 3,36 lít khí NO (đktc, sản phẩm khử duy nhất). Giá trị của m là
Cho các sơ đồ phản ứng sau:
1. C + O2 CO2. 4. C + H2 CH4.
2. C + CuO Cu + CO. 5. C + H2SO4 (đặc) SO2 + CO2 + H2O.
3. C + Ca CaC2. 6. C + H2O CO + H2.
Các phản ứng cacbon thể hiện tính oxi hóa là
Cho các sơ đồ phản ứng sau:
1. C + O2 CO2. 4. C + H2 CH4.
2. C + CuO Cu + CO. 5. C + H2SO4 (đặc) SO2 + CO2 + H2O.
3. C + Ca CaC2. 6. C + H2O CO + H2.
Các phản ứng cacbon thể hiện tính oxi hóa là